- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Влияние генотипа на фенотип
Одним из интересных моментов в исследовании ОНП является изучение механизмов влияния замещённого нуклеотида на транскрипцию и трансляцию. Известно, что аминокислоты, образующие белок, кодируются в ДНК тремя последовательными нуклеотидами, кроме того, существуют ещё специальные «старт» и «стоп» последовательности (рис. 1), которые регулируют процесс трансляции. каждую такую замену можно отнести к участку, находящемуся в гене или в межгенном пространстве.
Влияние ОНП относят к различным типам: химическое взаимодействие с окружением, влияние на трансляцию и транскрипцию, и т.д. Взаимодействие с окружением не несёт в себе какой-либо генетической информации, но меняет
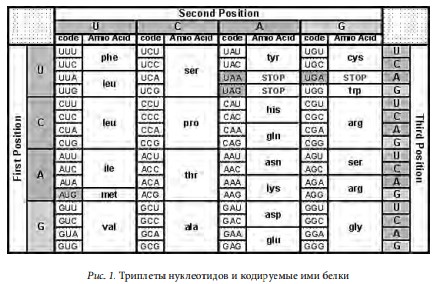
пространственное расположение ДНК, за счёт взаимодействия с другой частью цепи, или способствует присоединению различных сторонних компонентов (метилирование, фосфорилирование и пр.). Но такие изменения зачастую менее выражены в фенотипе, чем непосредственное влияние на трансляцию.
Известны случаи таких ОНП, которые меняют кодон одной аминокислоты в гене на другой, а также и на стоп/старт кодоны. В итоге при трансляции белок укорачивается (удлиняется) или возникает замена одной аминокислоты на другую. по всему миру ведётся поиск механизмов непосредственного влияния полиморфизмов для каждого из известных ОНП.
Например, в одном из исследований, проведённом в 2009 году, было найдено, что полиморфизм в +331 позиции гена PR приводит к замене аминокислоты в белке PMH, что существенно повышает риск возникновения рака молочной железы у женщин. Не стоит забывать, что в человеческом геноме в норме присутствуют две копии одного отрезка генома (парность хромосом), поэтому наличие одного минорного аллеля (гетерозигота) редко приводит к ранней смерти организма, с другой стороны, множество особей с гомозиготой ряда минорных аллелей не выживают.
Обнаружение такого пути взаимодействия для полиморфизмов, открытых статистическими методами (GWAS), является одним из самых достоверных способов подтверждения полученных результатов.
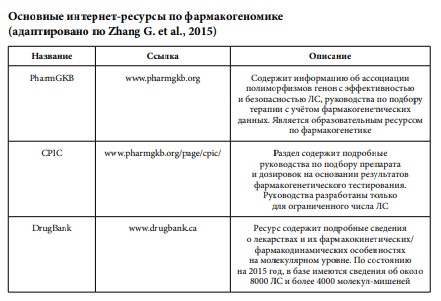
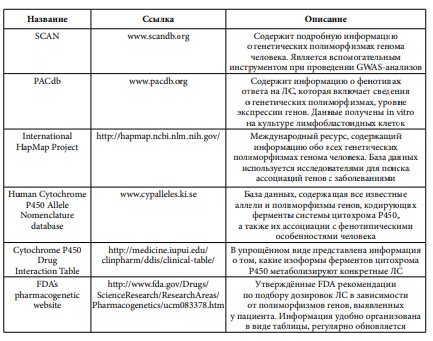
Для удобства обработки данных, полученных в экспериментах, биоинформатиками написано множество различных программ. На данный момент не существует какого-либо общего интерфейса, способного по генотипу человека выдавать всю имеющуюся информацию о предрасположенности к заболеваниям и других изменениях, которые могут проявиться у данного индивида.Перечислим общедоступные референсные базы данных по клинически значимым генетическим вариациям.
База данных OMIM
Online Mendelian In Heritancein Man — объединённый всемирный проект по хранению информации о заболеваниях, наследуемых по законам Менделя. Он содержит информацию о полиморфизмах и мутациях, которые когда-либо вызвали то или иное заболевание. Существенной трудностью является отсутствие какой-либо информации о вероятности повторения заболевания у другого лица, имеющего эту же мутацию или полиморфизм, для более чем половины записей в базе. также существует и техническая трудность обработки — база каталогизирована по генам, а не по мутациям.
В данной базе данных содержится информация о более чем 15 тысяч полиморфизмов и мутаций. Их можно разделить на следующие основные группы:
- Полиморфизмы, гарантированно вызывающие заболевания.
- Полиморфизмы, с OR>5. Вероятность возникновения заболевания при их наличии высокая;.
- Полиморфизмы и мутации, единожды вызвавшие то или иное заболевание, но для которых не ясно, может ли это повториться.
База данных SNPedia
SNPedia — свободная база данных, сделанная на основе Wikipedia, которая позволяет различным исследовательским группам добавлять информацию о влиянии полиморфизмов на возникновение заболевания.
После добавления новой информации сотрудники SNPedia оценивают качество данной информации и указывают «magnitude» — субъективную достоверность связи полиморфизма и болезни. записи, имеющие наибольшую достоверность, обычно имеют множество подтверждений от различных исследовательских групп. В базе хранится порядка 8000 полиморфизмов, но в большинстве своём они просто пересекаются с предыдущими базами. Их можно отнести к следующим группам:
- Полиморфизмы, с OR>5. Вероятность возникновения заболевания при их наличии высокая.
- Полиморфизмы, с OR<5. Вероятность возникновения заболевания при их наличии низкая, также они могут содержать в себе и протективный аллель.
- Полиморфизмы, содержащие в записи о себе информацию о риске, но не имеющие статистических записей, позволяющих привести абсолютные риски к относительным.
- Полиморфизмы, о которых известно лишь качественное влияние на признак без каких-либо количественных значений.
База данных LOVD
Leiden Open Variation Database— свободное программное обеспечение, позволяющее удобно хранить и предоставлять искателям информацию о мутациях, которые вызывают то или иное заболевание. каждая исследовательская группа, занимающаяся определённой патологией, может установить это пО и разместить в нём обнаруженные мутации. На данный момент существует порядка 40 различных отдельных проектов на основе LOVD, содержащих более 20 тысяч записей о мутациях.
Статьи по теме
- Генетическое тестирование при назначении психофармакотерапии
- Основные методики психических расстройств
- Назначение антипсихотиков
- Применение фармакогенетического тестирования при назначении антидепрессантов
- Показания для применения фармакогенетического теста при назначении антидепрессантов
- Факторы фармакодинамические и генетические
- Фармакокинетические факторы
- Полногеномные ассоциативные исследования GWAS
- Литий и циркадные ритмы
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

